ニュースリリース(詳細)
患者参画支援ソリューション 「Voicebook」
患者インタビューなど新たなサービスを提供開始
2023年9月1日
イーピーエス株式会社
イーピーエス株式会社(本社:東京都新宿区、代表取締役:佐々 明、以下 「EPS」)は、製薬企業の患者参画の取り組みに貢献するため、昨年10月に開始した「Voicebook」の「患者アンケートサービス」に加えて、新たに3つのサービス「患者インタビューサービス」、「PLS*1 作成サービス」、「患者参画コーディネーター資材レビューサービス」の提供を開始します。
患者さんと協働した医薬品開発
患者さんの声を収集し治験に反映することにより、治験参加者の負担軽減や治験への参加のしやすさを高めることに加え、製薬企業にとっては医薬品開発に新たな視点を与えることができます。日本においても、2022年12月23日に ICH-E8*2(R1)が発出されたことにより、患者さんの視点が医薬品開発のすべての段階を通して有意義になり得る、という考えが浸透しつつあります。さらに ICH-E6*3(R3)もステップ3となり、患者さんからのインプットが求められていくことが示唆されます。

患者参画支援ソリューション 「Voicebook」
「Voicebook」 は、患者さんの声を重視した医薬品開発や患者さんへの情報提供に貢献する患者参画支援ソリューションです。
治験参加者へアンケートを実施するサービスとして EPS が昨年開始したこの 「Voicebook」 は、この度、同じ EPS グループで国内最大手の SMO である株式会社 EP 綜合(以下 「EP 綜合」)の支援を受け、新たに3つのサービスの提供を開始します。EPS が本ソリューションの全体マネジメントを担い、高度な専門知識を備えた CRC を多数擁する EP 綜合と連携して患者参画に取り組みます。
■「Voicebook」 の4つのサービス
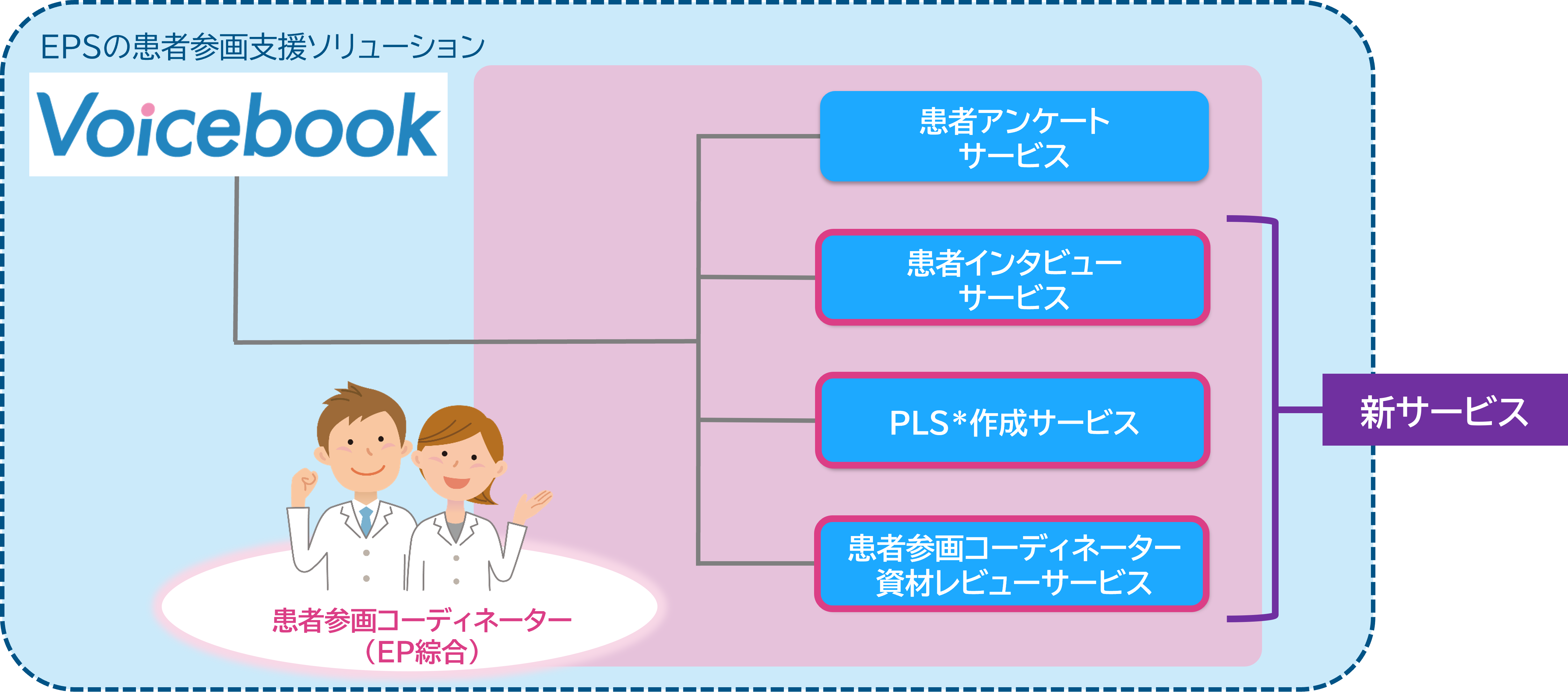
- 患者アンケートサービス
Web システムを用いて治験参加者からアンケートで幅広い声を収集します。 - 患者インタビューサービス
患者参画コーディネーターが患者さんに寄り添ったインタビューで生の声を収集します。 - PLS 作成サービス
CSR*4 を元に、EPS のメディカルライターが、わかりやすい PLS を作成します。 - 患者参画コーディネーター資材レビューサービス
患者参画コーディネーターが「患者向け資材」のわかりやすさをレビューします。
■「Voicebook」 の3つの強み
- 患者参画の専門職である「患者参画コーディネーター」
EP 綜合に所属する臨床試験の十分な経験を有する治験コーディネーターが「患者参画コーディネーター」として、医薬品開発に協働いただける患者さんと製薬企業との懸け橋を担います。 - CRO*5・ SMO*6 の立場を活かした患者参画活動支援
直接的な利害関係のない立場で、患者さんの本音を偏りなく引き出します。 - CRO と SMO の強みを融合したトータルサポート
EPS と EP 綜合の合同専門チームが、それぞれの豊富な実績で培ったノウハウを活かし、企画段階から、患者さんの選定・インタビューの対応・レポート作成等までトータルサポートします。
「Voicebook」 は、製薬企業が、医薬品開発等のパートナーである患者さんの声を直接的に聞くことができる機会を提供し、治療に関する患者さんのニーズをより深く理解することを支援します。これにより、医薬品開発に新たな視点が加わり、より価値の高い医薬品開発に貢献します。
EPS は、今後も 「Voicebook」 の新サービスを拡充し、製薬業界の患者参画をさらに推進して健康産業の発展に寄与します。
イーピーエス株式会社について
イーピーエス株式会社は1991年に事業を開始し、治験や PMS*7を中心とした臨床試験を総合的に支援する CRO です。臨床試験を推進する機能のすべての入口となる 「Trial GATE」 というコンセプトに基づき、様々な領域、フェーズの試験において医療機関や患者さんと製薬企業の橋渡しとなり、患者中心の治験の在り方を追求して参ります。
株式会社EP綜合について
EP 綜合は、SMO として、治験実施施設(医療機関)と契約し、GCP*8 に基づき適正な治験実施ができるよう、医療機関における治験業務を支援しています。治験に関わる医師や看護師、事務局の皆様の業務をサポートし、負担軽減および品質・スピード向上を実現します。
近年は IT 技術を活用した治験業務の効率化を積極的に進めており、治験の依頼者である製薬企業と実施フィールドとなる医療機関との橋渡し役として、それぞれのニーズを具現化するサービスを提供し、更なる治験実施環境の向上を推進しています。
患者参画
PPI*9 とも呼ばれます。
PMDA*10 は、患者さん等の声を把握、理解し、業務に活用することを患者参画と定義し、患者参画により ”Patient First” という取り組みを具現化するとともに、患者さん等の薬事行政に対する理解と満足度の向上を図ることを目指すと述べています。また、AMED*11 によれば、「研究への患者・市民参画(PPI)」 とは医学研究・臨床試験プロセスの一環として、研究者が 患者・市民(患者さん、家族、元患者さん(サバイバー)、未来の患者さんを想定)の知見を参考にすることとされています。
米国の FDA*12 においては、患者さんに焦点を当てた医薬品開発(PFDD*13)は患者さんの経験や視点、ニーズ、および優先度等を把握し、医薬品の開発と評価に有意義に組み込むための体系的なアプローチとされています。
【本件に関するお問い合わせ先】
イーピーエス株式会社 広報戦略室
E-mail:koho@eps.co.jp
- *1 PLS:Plain Language Summaries(治験参加者やご家族に対し、治験結果についてわかりやすい表現を用いて情報提供を行うことを目的とした文書)
- *2 ICH-E8:General Considerations for Clinical Trials(臨床試験の一般指針)
- *3 ICH-E6:GOOD CLINICAL PRACTICE (GCP)(医薬品の臨床試験の実施に関する基準のガイドライン)
- *4 CSR:Clinical Study Report(治験総括報告書)
- *5 CRO:Contract Research Organization(医薬品開発業務受託機関)
- *6 SMO:Site Management Organization(治験施設支援機関)
- *7 PMS:Post Marketing Surveillance(製造販売後調査)
- *8 GCP:Good Clinical Practice(医薬品の臨床試験の実施の基準に関する省令)
- *9 PPI:Patient and Public Involvement(患者・市民参画)
- *10 PMDA:Pharmaceuticals and Medical Device Agency(医薬品医療機器総合機構)
- *11 AMED:Japan Agency for Medical Research and Development(日本医療研究開発機構)
- *12 FDA:Food and Drug Administration(アメリカ食品医薬品局)
- *13 PFDD:Patient-focused Drug Development(患者に焦点を当てた医薬品開発)
