申請関連アウトソーシング(eCTD、Gateway)
医薬品の承認申請を豊富な経験でトータルサポート
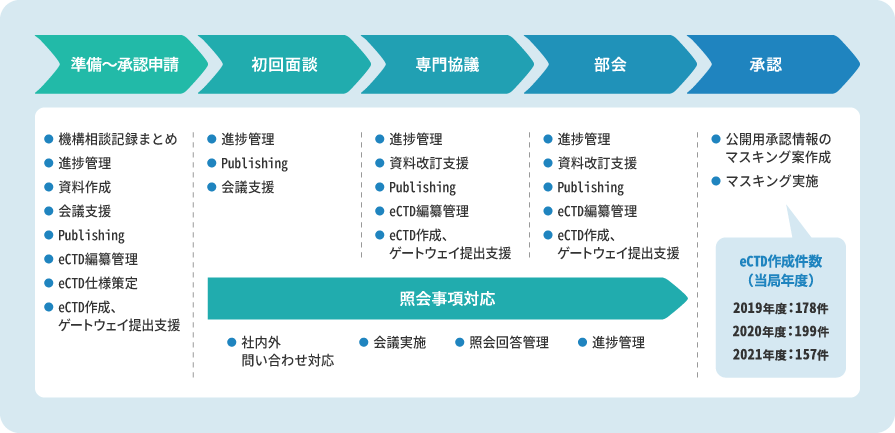
申請電子データ作成から、メディカルライティング、eCTD編纂・提出まで対応可能です。
eCTD作成支援ではトップクラスの実績件数があり、豊富な経験とノウハウを基に、安心してお任せいただける申請関連アウトソーシングサービスをご提供しています。
また、2020年5月には、いち早くeCTD v4.0関連のサービスも開始しております。v4.0での申請も引き続き当社にお任せください。
EPSの特徴
長年の実績に基づく品質の確保と保証
2005年と業界内でも早期にeCTD作成支援サービスを開始。そこから20年近くの実績を重ね、各作業工程では、そのノウハウを盛り込んだ標準チェックシートによりQC作業を実施しています。
年間のeCTD提出支援回数は150件を超え、ご依頼者さまから高い評価をいただいています。
また、CDISC標準データセットの作成においても、過去5年間でSDTM、ADaM共に250件以上の当局提出支援経験の実績がございます。eCTD v4.0における臨床試験データ提出のご不安も解消いたします。
承認申請の準備段階から承認取得までサポート
CTD M1資料の作成、QC、照会事項回答作成支援等、薬事部門の業務をご支援いたします。
また、豊富な業務経験をベースに、電子申請手順策定コンサルティングも行っており、eCTD v4.0移行に備えた社内体制・プロセス策定のご相談も可能です。
グローバルサブミッションへの対応
海外の申請関連業務のエキスパート企業やソフトウエアベンダーとパートナーシップを締結。3極(FDA、MHLW、EMA)のほか、アジアやその他各国への申請にも対応しています。
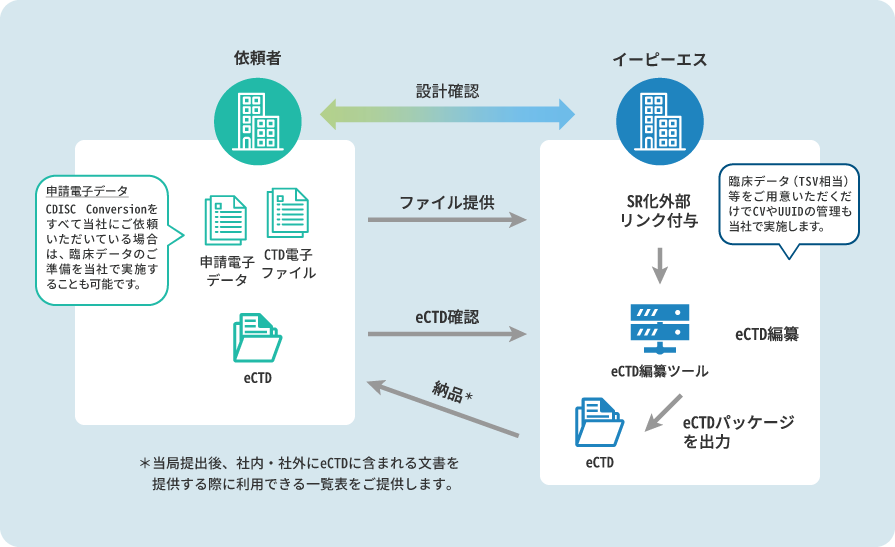
eCTDおよび臨床データのゲートウェイ提出への対応
eCTDおよび臨床データのゲートウェイ提出代行または提出立ち合いのどちらでも対応が可能です。ゲートウェイシステムに関する懸念や課題は、スタッフがその場で解決いたします。
サービス内容
eCTD v4.0 関連サービス
| サービス | 内容 |
|---|---|
| 1. eCTD v4.0 Publishing | 臨床データを含むeCTDの作成 |
| 2. Gateway Submission | ゲートウェイ提出にかかわる業務
|
| 3. 手順書作成支援 (申請対応アセスメント) |
規制対応プロセスの整備と手順書の作成
|
| 4. 教育・研修支援 | 手順教育の実施、教育用資料の作成・提供 |
| 5. システム導入・入れ替え支援 | v4.0に関連するシステムの導入および入れ替え |
申請関連アウトソーシングサービス